وبلاگ
خانه » مشخصات،خواص و کاربرد الکل ها

مشخصات،خواص و کاربرد الکل ها
الکلها دستهای از ترکیبات آلی هستند که با حضور یک یا چند گروه هیدروکسیل (-OH) متصل به یک اتم کربن مشخص میشوند. آنها ترکیبات متنوعی هستند که اهمیت قابل توجهی در صنایع مختلف، از جمله تولید مواد شیمیایی، داروسازی، انرژی و محصولات مصرفی دارند. الکلها یکی از بزرگترین گروهها درترکیبات شیمیایی میباشند و در واکنشهای زیادی شرکت میکنند. بخش عمدهای از ترکیبات شیمیایی از الکلها به وجود میآیند. معمولا هنگامیکه از نام الکل استفاده میشود، منظوراتانول است. اتانول مایعی بی رنگ و فرار است که بویی بسیار تند دارد و از تخمیر شکرها پدید میآید.
فهرست مطالب
Toggleتاریخچه الکلها
تاریخچه الکلها به حدود 10,000 سال پیش و عصر نوسنگی بازمیگردد، زمانی که انسانها با تخمیر طبیعی میوهها، عسل و غلات، نوشیدنیهای الکلی تولید میکردند، بدون اینکه درک علمی از ماهیت الکل داشته باشند. الکل، در قرون وسطی (قرن 8-9 میلادی) توسط دانشمندان اسلامی مانند جابر بن حیان و زکریای رازی توسعه یافت. زکریای رازی با تقطیر شراب در دستگاه انبیق (ابزاری کیمیاگری شبیه دستگاههای تقطیر امروزی) و قرع (ظرفی شبیه بالن آزمایشگاهی)، اتانول را خالصسازی کرد و آن را “الکحل” نامید که برای مقاصد پزشکی و دارویی استفاده شد. واژه “الکحل” بعدها به “الکل” در زبانهای اروپایی تبدیل شد. در قرون وسطی، دانش تقطیر به اروپا راه پیدا کرد و الکل در تولید مشروبات الکلی و داروسازی به کار رفت. امروزه، الکلها در صنایع مختلفی از جمله سوختهای زیستی، ضدعفونیکنندهها و تولید پلیمرها نقش کلیدی دارند.
مشخصات الکلها
تعریف و ساختار : الکلها مولکولهای آلی با فرمول کلی CnH2n+1OH برای الکلهای تکهیدریک (حاوی یک گروه هیدروکسیل) هستند. گروه هیدروکسیلی خواص منحصر به فردی به الکلها میدهد و آنها را از هیدروکربنها متمایز میکند. اتم کربن متصل به گروه -OH طبقهبندی الکلها را تعیین میکند:
- الکلهای نوع اول: کربنی که یک گروه -OH دارد و به یک اتم کربن دیگر متصل است مانند اتانول.CH3CH2OH
- الکلهای نوع دوم: کربنی که یک گروه -OH دارد به دو اتم کربن دیگر متصل است مانند ایزوپروپانول CH3CHOHCH3.
- الکلهای نوع سوم: کربنی که یک گروه -OH دارد به سه اتم کربن دیگر متصل است مانند ترت-بوتانول (CH₃)₃COH.
- الکلهای چند عاملی: حاوی چندین گروه هیدروکسیل هستند مانند گلیسرولC3H8O.

مشخصات الکلها
معرفی الکلها
فرمول عمومی آن به صورت R-OHR-OH میباشد. الکلها دارای گروه عاملی OH هستند که به اتم کربن متصل است. الکلها یکی از بزرگترین گروهها درترکیبات شیمیایی میباشند و در واکنشهای زیادی شرکت میکنند. بخش عمدهای از ترکیبات شیمیایی از الکلها به وجود میآیند. معمولا هنگامیکه از نام الکل استفاده میشود، منظوراتانول است. اتانول مایعی بی رنگ و فرار است که بویی بسیار تند دارد و از تخمیر شکرها پدید میآید.
انواع رایج الکلها
اتانول، اتیلن، ایزوپروپیل الکل و متانول، از جمله الکلهای پرکاربرد هستند. برخی الکلها مصرف طبی و برخی مصارف صنعتی دارند. الکل طبی همان اتانول است که دارای خلوص بالای %96 است و %4 آن را آب تشکیل میدهد. برای اینکه الکل ضدعفونیکننده باشد، باید درجه خلوصی بالای %70 داشته باشد. الکل صنعتی همان اتانول است و خلوص بسیار کمتری دارد. برای اینکه مردم الکلهای صنعتی و طبی را از یکدیگر تشخیص دهند و اشتباه مصرف نکنند، به اتانولهای با خلوص کمتر موادی رنگی و تلخکننده اضافه میکنند.
- متانول CH₃OH: سادهترین الکل، که با نام متیل الکل یا الکل چوب نیز شناخته میشود.
- اتانول C₂H₅OH: به عنوان اتیل الکل شناخته میشود و به طور گسترده در نوشیدنیها و به عنوان سوخت زیستی استفاده میشود.
- ایزوپروپانول CH3CHOHCH3: همچنین ایزوپروپیل الکل یا 2-پروپانول نامیده میشود و معمولاً به عنوان ضدعفونیکننده استفاده میشود.
- بوتانول C₄H₉OH: در ایزومرهای متعدد (n-بوتانول، سک-بوتانول، ترت-بوتانول) وجود دارد و به عنوان حلال و افزودنی سوخت استفاده میشود.
- گلیسرول C3H8O: یک الکل سه عاملی است که در لوازم آرایشی و دارویی استفاده میشود.
- اتیلن گلیکول C2H6O2: یک الکل دیهیدریک که به عنوان ضد یخ و در تولید پلیمر استفاده میشود.
نامگذاری الکل ها
الکلها با استفاده از سیستم آیوپاک نامگذاری میشوند، که در آن طولانیترین زنجیره کربنی حاوی گروه -OH شناسایی شده و پسوند “-ول” اضافه میشود. موقعیت گروه هیدروکسیل با یک عدد نشان داده میشود (به عنوان مثال، پروپان-2-ول برای ایزوپروپانول). برای الکلهای پلیهیدریک، پیشوندهایی مانند “-دی” یا ” -تری” تعداد گروههای هیدروکسیل را نشان میدهند (به عنوان مثال، پروپان-1،2،3-تریول برای گلیسرول).
-
روشهای تولید الکلها
الکلها به دو روش اصلی بیولوژیکی و صنعتی تولید میشوند:
-
تولید بیولوژیکی (تخمیر)
– فرآیند: قندها (مثل گلوکز) از نشاسته یا ساکاروز توسط آنزیمها (اینورتاز و زایماز) در دمای حدود 27 درجه سانتیگراد در کنار مخمر تخمیر میشوند:
– محصول: اتانول (8-15%) که با تقطیر خالص سازی میشود.
– کاربرد: نوشیدنیهای الکلی، سوخت زیستی.
-
تولید صنعتی
- هیدراتاسیون آلکنها:
– مستقیم: آلکن (مثل اتیلن) با آب و کاتالیزور اسیدی به الکل تبدیل میشود (مثل اتانول).
– غیرمستقیم: آلکن با اسید سولفوریک واکنش داده، استر سولفات تشکیل میدهد و سپس هیدرولیز به الکل (مثل ایزوپروپانول).
- واکنش جانشینی: آلکیل هالید باNaOH یا KOH به الکل نوع اول تبدیل میشود. نوع اول با سدیم هیدروکسید و یا پتاسیم هیدروکسید(واکنشهای جانشینی) به توليد الكل نوع اول منجر ميشود.
- کاهش آلدهیدها و کتونها: آلدهید به الکل نوع اول و کتون به الکل نوع دوم با عوامل کاهنده.
- فرآیند زیگلر: تولید الکلهای خطی (چرب) از اتیلن با تریاتیلآلومینیوم و هیدرولیز.
- هیدروفرمیلاسیون: آلکن با CO و H2 به آلدهید و سپس الکل تبدیل میشود.
نکات:
- تخمیر روشی پایدار برای اتانول است.
- روشهای صنعتی برای تولید الکلهای متنوع (مانند متانول، ایزوپروپانول) استفاده میشوند.
- فرآیندها ممکن است شامل مواد شیمیایی خطرناک یا انرژیبر باشند.
خواص فیزیکی الکلها
الکلهای سبک تر (متانول، اتانول و ایزوپروپانول) در دمای اتاق مایعات بیرنگ هستند، در حالی که الکلهای سنگین تر (به عنوان مثال، ستیل الکل) ممکن است به صورت جامدات مومی شکل ظاهر شوند. ظاهر آنها به وزن مولکولی و ساختار الکل بستگی دارد.
-
نقاط جوش و ذوب
الکلها به دلیل پیوند هیدروژنی موجود بین گروههای هیدروکسیل، نقاط جوش بالاتری نسبت به هیدروکربنهای با وزن مولکولی مشابه نشان میدهند. به عنوان مثال:
- متانول: نقطه جوش 64.7 درجه سانتیگراد
- اتانول: نقطه جوش 78.37 درجه سانتیگراد
- ایزوپروپانول: نقطه جوش 82.6 درجه سانتیگراد
- گلیسرول: نقطه جوش 290 درجه سانتیگراد (به دلیل گروههای -OH متعدد که پیوند هیدروژنی را تقویت میکنند)
نقطه جوش با وزن مولکولی در یک سری همولوگ افزایش مییابد. شاخهدار شدن در زنجیره کربنی (مثلاً در ایزوپروپانول در مقابل n-پروپانول) به دلیل کاهش سطح تماس برای برهمکنشهای بین مولکولی، نقطه جوش را کمی کاهش میدهد. نقطه ذوب نیز با افزایش طول زنجیره افزایش مییابد، به طوری که الکلهای سنگین تر مانند استئاریل الکل در دمای اتاق جامد هستند.
-
حلالیت
حلالیت الکلها در آب به طول زنجیره کربنی بستگی دارد:
الکلهای سبک تر (متانول، اتانول، ایزوپروپانول) به دلیل پیوند هیدروژنی قوی بین گروه -OH و مولکولهای آب، کاملاً در آب قابل امتزاج هستند.
الکلهای سنگین تر (مثلاً بوتانول و بالاتر) به دلیل غلبه زنجیره کربن آبگریز بر گروه هیدروکسیل آبدوست، حلالیت کمتری دارند. به عنوان مثال، n-بوتانول در دمای 25 درجه سانتیگراد تقریباً 7.4 گرم در 100 میلیلیتر آب حلالیت دارد.
الکلهای پلیهیدریک مانند گلیسرول و اتیلن گلیکول به دلیل داشتن گروههای هیدروکسیل متعدد، در آب بسیار محلول هستند.
-
چگالی
الکلها معمولاً چگالی کمتری نسبت به آب دارند، به جز الکلهای پلیهیدریک مانند گلیسرول (چگالی 1.26 گرم بر سانتیمتر مکعب). برای مثال:
- متانول: 0.792 گرم بر سانتیمتر مکعب
- اتانول: 0.789 گرم بر سانتیمتر مکعب
- ایزوپروپانول: 0.786 گرم بر سانتیمتر مکعب
-
بو
الکلهای سبکتر بوهای مشخصی دارند:
- متانول: تند، کمی تند
- اتانول: ملایم، دلپذیر
- ایزوپروپانول: قوی، کمی شیرین
الکلهای بالاتر ممکن است بوی مومی یا چرب داشته باشند، در حالی که الکلهای چند عاملی مانند گلیسرول بیبو هستند.
خواص شیمیایی الکلها:
-
اسیدیته
الکلها به دلیل قطبیت پیوند O-H که به گروه هیدروکسیل اجازه میدهد پروتون اهدا کند، اسیدیته ضعیفی دارند. اسیدیته با افزایش اندازه گروه آلکیل به دلیل اثر اهداکننده الکترون، که باز مزدوج (یون آلکوکسید) را پایدار میکند، کاهش مییابد.
-
اکسیداسیون:
رفتار اکسیداسیون به نوع الکل بستگی دارد:
الکلهای نوع اول را میتوان با استفاده از عوامل اکسیدکننده مانند پرمنگنات پتاسیم (KMnO) یا تریاکسید کروم (CrO) به آلدهیدها و سپس اسیدهای کربوکسیلیک اکسید کرد.
الکلهای نوع دوم با کتونها اکسید میشوند
الکلهای نوع سوم به دلیل عدم وجود اتم هیدروژن روی کربن حامل گروه -OH، در برابر اکسیداسیون مقاوم هستند.
-
آبزدایی
الکلها میتوانند در حضور یک کاتالیزور اسیدی قوی (مثلاً اسید سولفوریک ) در دماهای بالا آبزدایی شوند و آلکنها را تشکیل دهند. سهولت آبزدایی به ترتیب زیر است: الکل نوع سوم > ثانویه > اولیه، به دلیل پایداری واسطه کاربوکاتیون.
الکلها در حضور یک کاتالیزور اسیدی با اسیدهای کربوکسیلیک واکنش میدهند و استرها را تشکیل میدهند که به طور گسترده در عطرها، طعمدهندهها و پلاستیکها استفاده میشوند.
-
احتراق
الکلها قابل اشتعال هستند و در حضور اکسیژن دچار احتراق کامل میشوند و دی اکسید کربن و آب تولید میکنند. این ویژگی باعث میشود الکلهایی مانند اتانول و متانول به عنوان سوخت قابل استفاده باشند.

کاربردهای الکلها
کاربردهای صنعتی:
متانول:
- حلال: در رنگها، لاکها و چسبها استفاده میشود.
- سنتز شیمیایی: پیشساز فرمالدئید، اسید استیک و متیل استر.
- سوخت: در پیلهای سوختی و به عنوان افزودنی بنزین استفاده میشود.
- ضد یخ: از یخزدگی در سیستمهای صنعتی جلوگیری میکند.
اتانول:
- سوخت زیستی: مخلوط با بنزین برای کاهش انتشار گازهای گلخانهای.
- حلال: در عطرها، رنگها و جوهرها استفاده میشود.
- ماده واسطه شیمیایی: در سنتز اتیل استات و سایر ترکیبات استفاده میشود.
ایزوپروپانول:
- حلال: در مواد تمیزکننده، الکترونیک و پوششها رایج است.
- سنتز شیمیایی: برای تولید استون و سایر مواد شیمیایی استفاده میشود.
بوتانول:
- حلال: در لاکها و پوششها استفاده میشود.
- سوخت زیستی: n-بوتانول به دلیل محتوای انرژی بالاتر نسبت به اتانول، به عنوان یک سوخت زیستی نسل بعدی مورد بررسی قرار میگیرد.
-
کاربردهای پزشکی و دارویی
- اتانول و ایزوپروپانول:
-ضدعفونیکنندهها: در ضدعفونیکنندههای دست، دستمالهای مرطوب پزشکی و ضدعفونیکنندههای سطوح استفاده میشوند (70٪ اتانول یا ایزوپروپانول برای فعالیت ضدمیکروبی بهینه است).
حلال دارویی: در فرمولاسیونها و استخراجهای دارویی استفاده میشود.
- گلیسرول:
-ماده مرطوبکننده: در کرمها، لوسیونها و داروها برای حفظ رطوبت استفاده میشود.
-دارورسانی: به عنوان حلال یا تثبیتکننده در داروهای مایع استفاده میشود.
- اتیلن گلیکول:
-نگهدارنده پزشکی: در برخی از فرآیندهای نگهداری نمونههای بیولوژیکی استفاده میشود.
-
بخش انرژی
- اتانول: یک سوخت زیستی تجدیدپذیر تولید شده از زیستتوده (به عنوان مثال، ذرت، نیشکر). این ماده وابستگی به سوختهای فسیلی را کاهش میدهد و انتشار گازهای گلخانهای را کاهش میدهد.
- متانول: در سلولهای سوختی و به عنوان حامل هیدروژن برای کاربردهای انرژی پاک استفاده میشود.
- بوتانول: به عنوان یک سوخت زیستی با چگالی انرژی بالاتر و سازگاری بهتر با زیرساختهای سوخت موجود در حال ظهور است.
-
محصولات مصرفی
-
لوازم آرایشی و بهداشتی:
-گلیسرول به دلیل خاصیت مرطوبکنندگیاش در صابونها، مرطوبکنندهها و خمیردندانها استفاده میشود.
-اتانول در عطرها و دئودورانتها به عنوان حلال و حامل استفاده میشود.
-
پاککنندههای خانگی:
-ایزوپروپانول یک ماده کلیدی در شیشهپاککنها و اسپریهای ضدعفونیکننده است.
-اتانول در مواد تمیزکننده چندمنظوره استفاده میشود.
-
غذا و نوشیدنی:
-اتانول الکل اصلی در نوشیدنیهای الکلی (آبجو، شراب، مشروبات الکلی) است.
-گلیسرول به عنوان شیرینکننده و نگهدارنده در محصولات غذایی استفاده میشود.
-
سنتز شیمیایی
الکلها واسطههای حیاتی در تولید موارد زیر هستند
- استرها: در عطرها، طعمدهندهها و پلاستیکها استفاده میشوند (به عنوان مثال، پلیاتیلن ترفتالات از اتیلن گلیکول).
- اترها: به عنوان حلال و بیحسکننده استفاده میشوند.
- آلکیل هالیدها: در سنتز آلی استفاده میشوند.
اطلاعات عمومی الکل های پرکاربرد
- الكلهاي ساختاريافتهتر و پيچيدهتري در آمينواسيدها، شكر و اسيدهاي چرب وجود دارند.
- متانول و اتانول دو مورد از مهمترین الکلها در جهان هستند.
- از متانول به عنوان الکل صنعتی نام میبرند.
- متانول سمی است و اثر مخربی بر بینایی داشته و حتی از راه پوست هم جذب میشود.
- از متانول به عنوان ماده اولیه برای تولید فرمالدهید و رزینها استفاده میشود.
- الکلهای C6 تا C11 برای افزایش خاصیت پلاستیکی یا کاهش ویسکوزیته مواد به کار میروند.
- اتانول و ایزوپروپیل الکل کاربردهای فراوانی در مواد ضدعفونی دارند و با حلکردن چربیها و پروتئینهای موجود در باکتریها و ویروسها، آنها را از بین میبرند.
- ایزوپروپیل الکل با نامهای دیگری مانند ایزوپروپانولیا پروپانول2 یا الکل مالشی شناخته میشود.
- ایزوپروپیل الکل ترکیبی شیمیایی، بیرنگ، قابل اشتعال و بابویی بسیار قوی است.
- ایزوپروپیل الکل، ماده اصلی بسیاری از محصولات شیمیایی مثل ضد عفونیکنندهها، گندزداها و مواد شویندهها میباشد.
- اتیلن بعد از آمونیاک، دومین ماده کاربردی پایه درصنعت پتروشیمی دنیا میباشد.
- اتیلن، هورمونی گیاهی است و در رسیدن میوه ها، باز شدن شکوفهها وگلها و ریزش برگهای پاییزی نقش دارد.
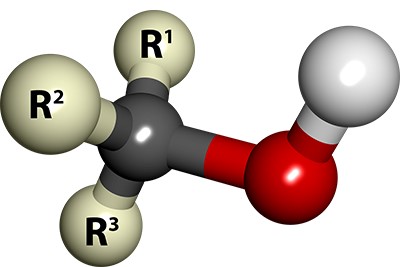
روش نامگذاری آیوپاک
معروفترین روش نامگذاری الکلها، روش ایوپاک میباشد ولی میتوان متناظر با گروه آلکیلی نیز، آنها را نامگذاری کرد. مراحل نامگذاری الکلها به این روش در ذیل آورده شده است:
- در نامگذاری الکلها به روش ایوپاک به انتهای نام آنها پسوند اُل ( ol ) افزوده میشود.
- برای مثال اتانول، ازآلکان داراید و کربن یعنی اتان ساخته شده است.
- برای نامگذاری ابتدا محل، تعداد و نام شاخه فرعی را میآوریم.
- بعد محل گروه متصل به OH را میآوریم.
- در نهایت نام شاخه اصلی را با پسوند اُل بیان میکنیم.
- در نامگذاری به روش دیگر، نام الکل متناظر با گروه آلکیل بیان میشود.

فرمول شیمیایی و ساختار الکلها
- وجود گروه هیدروکسیل، الکلها را قطبی میکند و باعث میشود تا این گروه با خودش و ترکیبات دیگر، پیوند هیدروژنی داشته باشد.
- وجود گروه OH سبب حلالیتپذیری بیشترالکلها نسبت به هیدروکربنها در آب است.
- متانول، اتانول و پروپانول در آب محلولاند.
- بوتانول با داشتن چهار اتم کربن در زنجیر کربنیش، تقریبا در آب محلول است.
- پیوند هیدروژنی موجود در الکلها سبب میشود تا آنها نسبت به هیدروکربنها و اِترها نقطه جوش بالاتری داشته باشند. برای مثال اتانول نقطه جوش بالاتری °C 78/29 نسبت به هگزان °C 69 دارد.
- الکلها دارای نیروهای هیدروژنی و بین مولکولی(واندروالسی و برهمکنش دوقطبی دوقطبی)میباشند.
- هرچقدر اندازه الکل بیشتر شود، نیروی واندوالس افزوده میشود. با افزایش طول مولکول و تعداد الکترونها، نیروی واندروالس قویتر میشود. با افزایش تعداد کربن، نقطه جوش بالاتر میرود.
- الکلهای کوچک در آب انحلالپذیری بالایی دارند و با هر نسبتی در آن حل میشوند.
- هرچه طول زنجیره هیدروکربنی افزایش یابد، انحلالپذیری الکل در آب کاهش مییابد.
نکات ایمنی کار با الکلها
در کار با الکلها باید نکات ایمنی زیادی را رعایت نمود. برای مثال باید در محیطهای آزمایشگاهی حتی الامکان از شوخی اجتناب نمایید و در آن محیط چیزی نیاشامید و نخورید. همچنین، دقت نمایید تا با دستکش از آن محیط خارج نشوید. در زمانی که ظروف حاوی مواد سمی را باز مینمایید، هود را روشن نمایید. مواد اشتعالزایی مثل الکل را از نزدیکی حرارت و شعله، دور نگه دارید. تا جایی که ممکن است مانع شوید تا مواد شیمیایی با پوست شما تماس پیدا کند و در صورت تماس موضع را با مقدار زیادی آب بشویید. در ادامه برخی از این نکات ایمنی ذکر شده است:
- استشمام مداوم مواد ضد عفونی کننده برای ریهها مضر است. از بوکردن این مواد بپرهیزید.
- هنگام استفاده از مواد ضد عفونیکننده حتما از دستکش استفاده نمایید.
- الکل را به صورت مستقیم به پوست نزنید و حتما آن را با مقدار معینی آب مقطر یا آب اکسیدان ترکیب نمایید.
- دستمال، پارچه و مواد نظافتی را بعد از آغشتهشدن به الکل در ظروف دربسته نگهداری کنید و در اولین فرصت دور بیاندازید.
- اگر مواد الکلی مشتعل شدند، با استفاده از آب و وسایل خاموش کننده، آتش را فرو نشانید.
- الکلها را به دلیل قابلیت اشتعال در محیط خنک نگهداری نمایید.
- ظروف شیشهای حاوی الکل را در قفسهها و ارتفاع بالا نگذارید. ممکن است به علت سقوط و شکسته شدنشان، حادثهساز شوند.
- قبل از مصرف این نوع مواد در داخل ماشین، پنجرهها را باز نمایید و چند دقیقه از روشن کردن خودرو خودداری کنید.
- بخارات الکل متانول سمی است در صورت تماس دستها را با آب بشویید.
- از تماس دستها با الکل متانول خودداری کنید. الکل متانول به سرعت از طریق پوست جذب میشود.
تفاوت روغن سرخ کردنی و روغن پخت و پز: تحلیل علمی و عملی
مقدمه روغنها از مهمترین اجزای آشپزی هستند که نقش اساسی در طعم، بافت و ارزش غذایی غذا ایفا میکنند. با
مواد تشکیلدهنده نرمکننده لباس و نقش هر کدام
مقدمه نرمکننده لباس یکی از محصولات اصلی در مراقبت از منسوجات به شمار میآید که هدف آن ایجاد لطافت، خوشبو
ایزوپروپیل الکل و نقش آن در شویندهها
چکیده ایزوپروپیل الکل Isopropyl Alcohol یا IPA یکی از پرمصرفترین الکلهای آلی در صنایع شیمیایی، دارویی و بهداشتی است. این
مواد کیلیتکننده چیست؟
مواد کیلیتکننده (Chelators یا Ligands) ترکیباتی هستند که توانایی دارند با یونهای فلزی آزاد پیوند برقرار کرده و آنها را